Questões de Química - Combustão - 2011
Limpar pesquisa
Questão: 1 de 8
201988

Banca: CESPE / Cebraspe
Órgão: CBM/DF
Cargo(s): Bombeiro Militar Operacional
Ano: 2011
Matéria/Assunto: Química > Termoquímica / Combustão
hematita (Fe2O3) e a magnetita (Fe3O4), e o ferro bruto é obtido, em
altos fornos siderúrgicos, a partir de reações do minério de ferro
com CO(g).
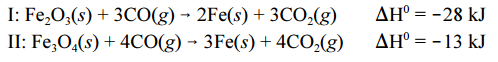
O CO(g) é produzido a partir da reação do O2 (g) da atmosfera com
um eletrodo de carbono, na forma de grafite.
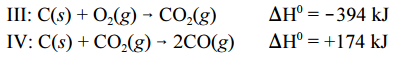
Com base nessas informações e considerando )H0 a variação de
entalpia padrão das reações a 25 ºC, julgue os itens a seguir.
Questão: 2 de 8
130445

Banca: CESPE / Cebraspe
Órgão: CBM/DF
Cargo(s): Bombeiro Militar - Condutor/Operador de Viaturas
Ano: 2011
Matéria/Assunto: Química > Termoquímica / Combustão
grande quantidade de queimadas da vegetação durante o inverno no DF. Essa umidade pode ser medida em termos absolutos ou
relativos. A umidade absoluta fornece uma medida da massa de
água por unidade de volume de ar ou por unidade de massa de ar. Já a umidade relativa é definida como a razão, expressa em
porcentagem, entre a concentração de água presente em
determinado volume de ar atmosférico e a concentração máxima
que pode estar presente, nesse mesmo volume e à mesma
temperatura, sem que ocorra condensação do vapor de água.
Com base nas informações acima apresentadas, considerando o
comportamento ideal para todos os gases, o fato de a densidade da
água, a 20 ºC, ser igual a 1,0 g/mL e sabendo que a condensação do
vapor de água contido no ar atmosférico, a 20 ºC, ocorre quando a
umidade absoluta atinge 17,0 g/m3, julgue os próximos itens.
Questão: 3 de 8
129238

Banca: CESPE / Cebraspe
Órgão: CBM/ES
Cargo(s): Oficial Bombeiro Militar Combatente
Ano: 2011
Matéria/Assunto: Química > Termoquímica / Combustão
que ocorra, é necessário misturar um combustível com um
comburente e fornecer uma energia de ativação, que pode ser chama
aberta, faísca ou centelha elétrica. A combustão de uma quantidade
padrão de determinado material libera uma quantidade de energia
denominada calor de combustão ou poder calorífico. Na tabela a
seguir, apresenta-se o poder calorífico de alguns combustíveis
usuais.
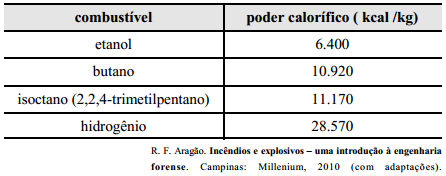
Com base nas informações acima apresentadas, julgue os itens que
se seguem.
Questão: 4 de 8
129204

Banca: CESPE / Cebraspe
Órgão: CBM/ES
Cargo(s): Oficial Bombeiro Militar Combatente
Ano: 2011
Matéria/Assunto: Química > Termoquímica / Combustão
que ocorra, é necessário misturar um combustível com um
comburente e fornecer uma energia de ativação, que pode ser chama
aberta, faísca ou centelha elétrica. A combustão de uma quantidade
padrão de determinado material libera uma quantidade de energia
denominada calor de combustão ou poder calorífico. Na tabela a
seguir, apresenta-se o poder calorífico de alguns combustíveis
usuais.

Com base nas informações acima apresentadas, julgue os itens que
se seguem.
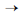 2CO + 3H2O expressa
corretamente a reação de combustão completa do etanol.
2CO + 3H2O expressa
corretamente a reação de combustão completa do etanol.Questão: 5 de 8
129206

Banca: CESPE / Cebraspe
Órgão: CBM/ES
Cargo(s): Oficial Bombeiro Militar Combatente
Ano: 2011
Matéria/Assunto: Química > Termoquímica / Combustão
que ocorra, é necessário misturar um combustível com um
comburente e fornecer uma energia de ativação, que pode ser chama
aberta, faísca ou centelha elétrica. A combustão de uma quantidade
padrão de determinado material libera uma quantidade de energia
denominada calor de combustão ou poder calorífico. Na tabela a
seguir, apresenta-se o poder calorífico de alguns combustíveis
usuais.

Com base nas informações acima apresentadas, julgue os itens que
se seguem.
