Questões de Geometria Molecular
Limpar pesquisa
Questão: 46 de 99
124292

Banca: CESPE / Cebraspe
Órgão: ANP
Cargo(s): Especialista em Regulação de Petróleo e Derivados, Álcool Combustível e Gás Natural - Área V
Ano: 2013
Matéria/Assunto: Química > Química Geral e Inorgânica / Geometria Molecular, Polaridade e Forças Intermoleculares
Questão: 47 de 99
113035

Banca: CESPE / Cebraspe
Órgão: CBM/ES
Cargo(s): Policial Militar - Soldado Combatente
Ano: 2011
Matéria/Assunto: Química > Química Geral e Inorgânica / Geometria Molecular, Polaridade e Forças Intermoleculares
livre, ele é responsável, direta ou indiretamente, por diversas patologias. Em termos químicos, esse óxido é fracamente reativo, porém exerce papel
deletério no organismo, por ser capaz de transpor facilmente membranas
celulares e gerar o radical hidroxil (•OH), seja por meio de exposição à luz ultravioleta (equação I), seja por interação com metais de transição, como o ferro, por meio do processo conhecido como reação de fenton (equação II).
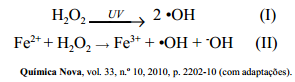
Considerando as informações acima, julgue os itens a seguir.
destaca a característica predominantemente apolar do peróxido de
hidrogênio.
Questão: 48 de 99
602679

Banca: FGV
Órgão: SEDUC/RN
Cargo(s): Professor - Química
Ano: 2025
Gabarito: Oficial
Matéria/Assunto: Química > Química Geral e Inorgânica / Geometria Molecular, Polaridade e Forças Intermoleculares
as ligações covalentes não polares ocorrem quando há uma grande diferença de eletronegatividade entre os átomos, resultando em uma distribuição de carga uniforme.
as forças de Van der Waals são interações intermoleculares fortes que ocorrem entre moléculas polares, devido à atração entre dipolos permanentes.
a ligação de hidrogênio é uma interação intermolecular que ocorre quando um átomo de hidrogênio, ligado a um átomo eletronegativo, é atraído por outro átomo eletronegativo de uma molécula diferente.
as moléculas polares têm pontos de ebulição mais baixos que as não polares, devido às interações intermoleculares mais fracas.
os sais são miscíveis em solventes apolares como hexano e tetraclorometano.
Questão: 49 de 99
578488

Banca: IBFC
Órgão: CBM/SE
Cargo(s): Cadete - Aluno Oficial
Ano: 2018
Gabarito: Oficial
Matéria/Assunto: Química > Química Geral e Inorgânica / Geometria Molecular, Polaridade e Forças Intermoleculares
I, II e III, apenas
I e II, apenas
II e III, apenas
III e IV, apenas
Questão: 50 de 99
577505

Banca: CESGRANRIO
Órgão: TRANSPETRO
Cargo(s): Técnico de Dutos
Ano: 2023
Gabarito: Oficial
Matéria/Assunto: Química > Química Geral e Inorgânica / Geometria Molecular, Polaridade e Forças Intermoleculares
2
4
8
10
12
