Questões de Química - Cinética química
Limpar pesquisa
Questão: 16 de 94
416130

Banca: FGV
Órgão: Pref. São Paulo/SP
Cargo(s): Professor - Química | Professor de Ensino Fundamental II e Médio
Ano: 2016
Matéria/Assunto: Química > Ligações e Transformações Químicas
7,82.
6,56.
1,02.
0,824.
0,122.
Questão: 17 de 94
415979

Banca: FGV
Órgão: SEDUC/PE
Cargo(s): Professor - Química
Ano: 2016
Matéria/Assunto: Química > Cinética química
5 minutos.
25 minutos.
50 minutos.
75 minutos.
100 minutos.
Questão: 18 de 94
409949

Banca: CESPE / Cebraspe
Órgão: PF
Cargo(s): Policial Federal - Papiloscopista
Ano: 2021
Matéria/Assunto: Química > Cinética química
digitais faz uso de pós. A interação dos pós com os componentes
da impressão digital se dá, normalmente, por interação de Van
der Waals. É comum utilizar óxido de ferro (III) — Fe2O3 — na
formulação desses pós. A revelação da impressão feita com
Fe2O3 pode ser destruída pela presença de ácido, por causa da
seguinte reação.
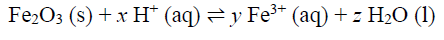
Com base nessas informações, julgue o seguinte item.
Questão: 19 de 94
407367

Banca: IDECAN
Órgão: IF/PB
Cargo(s): Professor - Química
Ano: 2019
Matéria/Assunto: Química > Cinética química
A velocidade de uma reação química geralmente cresce com o aumento da temperatura.
A velocidade de uma reação química sempre independe da concentração dos reagentes.
A velocidade de uma reação química independe da orientação apropriada das moléculas na hora do choque.
No caso dos sólidos, quanto menor a superfície de contato, maior será a velocidade da reação química.
Os catalisadores homogêneos geralmente são sólidos em contato com reagentes gasosos ou líquidos.
Questão: 20 de 94
407357

Banca: IDECAN
Órgão: IF/PB
Cargo(s): Professor - Química
Ano: 2019
Matéria/Assunto: Química > Cinética química
Estado físico dos reagentes; Área de contato entre reagentes.
Área superficial; Concentração dos produtos.
Concentração dos reagentes; Presença de catalisador.
Temperatura da mistura reacional; Área de contato entre reagentes.
Presença de catalisador; Estado físico dos reagentes.
